近日,学院王显祥教授团队联合动物营养所伍爱民副教授,在炎症性肠病口服靶向治疗领域取得研究进展,成功开发出可口服的结肠靶向 Cu-Mn₃O₄纳米酶水凝胶微球(HMCM)。该复合材料可保护纳米酶顺利通过胃酸、精准抵达结肠炎症部位,通过清除活性氧、抑制结肠上皮细胞铁死亡和调节肠道菌群的多重作用实现炎症性肠病治疗,为该疾病的临床治疗提供了全新的靶向给药策略。相关研究成果发表于中科院 1 区 TOP 期刊《Materials Today Bio》,论文题为《Multifunctional Cu-doped Mn₃O₄ nanozyme hydrogel microspheres for oral targeted treatment of inflammatory bowel disease》,全文链接:https://doi.org/10.1016/j.mtbio.2026.102932。学院王显祥教授与动物营养所伍爱民副教授为论文共同通讯作者,理学院生物资源化学专业2023级硕士研究生范维为第一作者。
炎症性肠病(IBD)是困扰全球超 680 万人的慢性疾病,患者常伴随腹痛、腹泻、便血等症状,严重影响生活质量。目前口服抗炎药物是该疾病的一线治疗方案,但临床应用中仍面临诸多难题,如药物靶向性差、生物利用度低,且难以有效清除肠道内过量的活性氧(ROS),治疗效果受限。针对这一临床痛点,研究团队创新地将 Cu-Mn₃O₄纳米酶(CM NZs)封装于藻酸钙水凝胶微球(HM)中,构建出具有结肠靶向特性的纳米酶水凝胶微球复合材料 HMCM,专门用于炎症性肠病的口服靶向治疗。
该复合材料的核心优势在于靶向递送与多重治疗功能的高效结合。一方面,Cu-Mn₃O₄纳米酶中的混合价态锰离子(Mn²+/Mn³+)与铜离子(Cu+/Cu²+),赋予其卓越的超氧化物歧化酶(SOD)、过氧化氢酶(CAT)及谷胱甘肽过氧化物酶(GPx)三重模拟活性,可实现对肠道内活性氧(ROS)的高效广谱清除;另一方面,藻酸钙水凝胶微球可抵御胃液的降解作用,确保纳米酶在体内稳定递送,并在结肠微环境中特异性溶解,实现 CM NZs 向结肠炎症部位的精准释放。在 DSS 诱导的结肠炎动物模型实验中,HMCM 展现出显著的治疗效果:可有效减轻肠道氧化应激,促进巨噬细胞从促炎 M1 型向抗炎 M2 型极化,精准调控炎症因子水平(TNF-α、IL-1β、IL-6、IL-10);同时能上调紧密连接蛋白(Claudin、ZO-1、Occludin)表达,修复肠道黏膜屏障,抑制结肠上皮细胞铁死亡,并重塑肠道菌群稳态,从多个维度实现结肠炎的有效治疗。此外,系统的安全性评估证实,HMCM 具有良好的生物相容性,不会在机体其他器官中蓄积,无明显毒性风险,符合生物医用材料的应用要求。
此次研发的多功能 HMCM 作为精准靶向结肠的给药平台,设计精巧且兼具安全性与高效性,不仅为炎症性肠病的口服靶向治疗提供了全新策略,也为动物肠道营养领域的相关研发开拓了新的思路与方向,展现出极具潜力的应用前景。
全文链接:https://doi.org/10.1016/j.mtbio.2026.102932
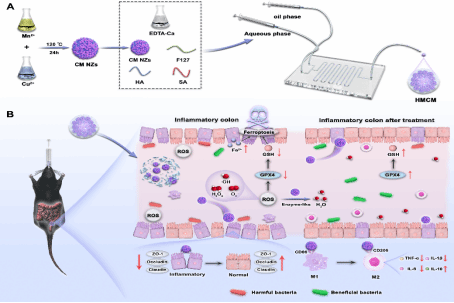
图 HMCM制备和IBD治疗机制的示意图